
Inhoud
Het massapercentage bepaalt het percentage van elk element dat een chemische verbinding vormt. Om deze waarde te vinden, hebt u de molaire massa van de samengestelde elementen in gram / mol nodig of het aantal grammen dat is gebruikt om de oplossing te maken. Het massapercentage kan op een eenvoudige manier worden berekend met behulp van een basisformule die de massa van het element (of opgeloste stof) deelt door de massa van de verbinding (of oplossing).
Stappen
Methode 1 van 2: Het massapercentage met gegeven massa's vinden
- Definieer de vergelijking voor het massapercentage van een verbinding. De basisformule voor een verbinding is: massapercentage = () x 100. U moet het resultaat aan het einde met 100 vermenigvuldigen om de waarden als percentages uit te drukken.
- De massa van een chemische verbinding waarin u geïnteresseerd bent, is de massa die in het probleem wordt gegeven. Als deze waarde niet wordt opgegeven, raadpleegt u de volgende methode en leert u hoe u het massapercentage kunt vinden wanneer de massa niet wordt gegeven.
- De totale massa van een verbinding wordt berekend door de massa van alle elementen die zijn gebruikt om de verbinding of de oplossing te maken, op te tellen.
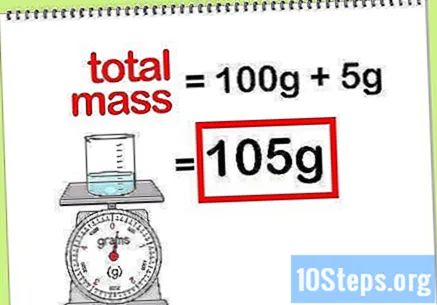
Bereken de totale massa van de verbinding. Als u de massawaarde kent van alle elementen of verbindingen die worden toegevoegd, hoeft u ze alleen maar op te tellen om de massa van de verbinding of de uiteindelijke oplossing te berekenen. Deze waarde is de noemer bij de berekening van het massapercentage.- Bijvoorbeeld: Wat is het massapercentage van 5 g natriumhydroxide opgelost in 100 g water?
- De totale massa van de verbinding is de hoeveelheid natriumperoxide plus de hoeveelheid water: 100 g + 5 g, in totaal dus 105 g.

Identificeer de massa van de chemische stof in kwestie. Wanneer u het percentage massa, wil het probleem dat je de massa van een specifiek element (het element in kwestie) vindt als een percentage van de totale massa van alle elementen. Let op de massa van het betreffende element. Deze waarde is de teller bij de berekening van het massapercentage.- De massa van het element is bijvoorbeeld 5 g natriumhydroxide.
- Vervang de variabelen in de massapercentageformule. Nadat u de waarden voor elke variabele hebt bepaald, vervangt u ze in de vergelijking.
- Bijvoorbeeld: massapercentage = () x 100 = () x 100.

Bereken het massapercentage. Nu de vergelijking is gevormd, los je deze op om het massapercentage te berekenen. Verdeel de massa van het element door de totale massa van de verbinding en vermenigvuldig met 100. Het resultaat is het massapercentage van het chemische element.- Bijvoorbeeld: () x 100 = 0,04761 x 100 = 4,751%. Het massapercentage van 5 g natriumhydroxide opgelost in 100 g water is dus 4,751%.
Methode 2 van 2: Het massapercentage vinden met niet-opgegeven massa's
- Definieer de vergelijking voor het massapercentage van een verbinding. De basisformule voor het massapercentage van een verbinding is: massapercentage = () x 100. U moet het resultaat aan het einde met 100 vermenigvuldigen om de waarden als percentages uit te drukken.
- Als u de massawaarden niet kent, kunt u het massapercentage van een element van de verbinding vinden met behulp van de molaire massa.
- Bijvoorbeeld: Wat is het massapercentage waterstof in een watermolecuul?.
Schrijf de chemische formule. Als de chemische formules voor elke verbinding niet worden verstrekt, moet u deze opschrijven. Ga anders verder met stap "Vind de massa van elk element".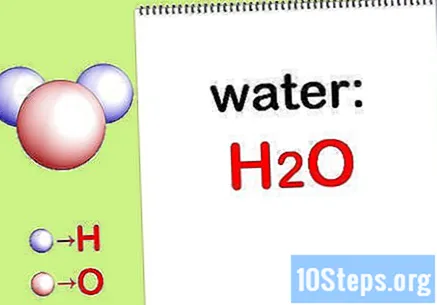
- Schrijf bijvoorbeeld de chemische formule voor water: H.2DE.
Zoek de massa van elk element in de compound. Zoek het molecuulgewicht van elk element van de chemische formules door naar het periodiek systeem te verwijzen. Over het algemeen is de massa van een element te vinden onder het symbool van het chemische element. Let op de massa van elk element van de verbinding.
- De molecuulmassa van zuurstof is bijvoorbeeld 15,9994 en die van waterstof is 1,0079.
Vermenigvuldig de massa's met de molaire verhouding. Bepaal hoeveel mol van elk element er in de chemische verbinding zitten. Het aantal mol wordt gegeven door het onderschreven nummer van de compound. Vermenigvuldig de moleculaire massa van elk element met de molaire verhouding.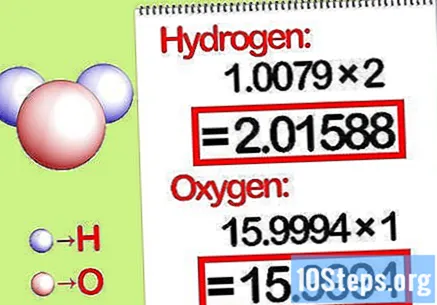
- De molaire verhouding van waterstof tot zuurstof in water is bijvoorbeeld 2: 1. Vermenigvuldig daarom het molecuulgewicht van waterstof met twee (1,00794 X 2 = 2,01588) en laat het molecuulgewicht van zuurstof zoals het is (15,9994).
Bereken de totale massa van de verbinding. Voeg de totale massa van alle elementen van de verbinding toe. Met behulp van de massa berekend door de molaire verhouding, is het mogelijk om de totale massa van de verbinding te berekenen. Dit getal is de noemer van de massapercentagevergelijking.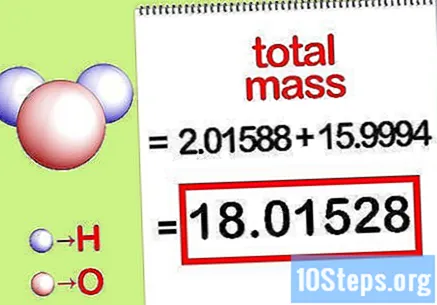
- Voeg bijvoorbeeld 2,01588 g / mol (de massa van twee mol waterstofatomen) toe met 15,9994 g / mol (de massa van een enkele mol van een zuurstofatoom) en verkrijg 18,01528 g / mol.
Identificeer de massa van het element in kwestie. Wanneer u het percentage massa, wil het probleem dat je de massa van een specifiek element in een verbinding vindt als percentage van de totale massa van alle elementen. Identificeer de massa van het betreffende element en schrijf het op. Het is de massawaarde berekend met behulp van de molaire verhouding. Deze waarde is de teller van de massapercentagevergelijking.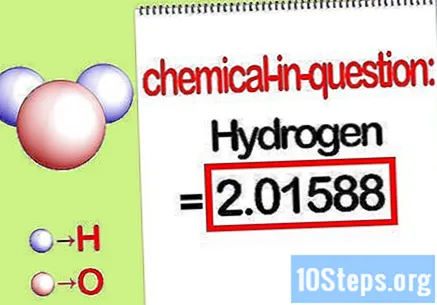
- De waterstofmassa van de verbinding is bijvoorbeeld 2,01588 g / mol (de massa van twee mol waterstofatomen).
- Vervang de variabelen in de massapercentageformule. Nadat u de waarden voor elke variabele hebt bepaald, vervangt u ze in de vergelijking die in de eerste stap is gedefinieerd: massapercentage = () x 100.
- Bijvoorbeeld: massapercentage = () x 100 = () x 100.
Bereken het massapercentage. Nu de vergelijking is gevormd, los je deze op om het massapercentage te berekenen. Verdeel de massa van het element door de totale massa van de verbinding en vermenigvuldig met 100. Het resultaat is het massapercentage van het chemische element.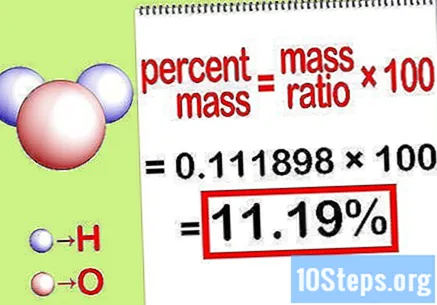
- Bijvoorbeeld: massapercentage = () x 100 = 0,111189 x 100 = 11,18%. Het massapercentage van waterstofatomen in een watermolecuul is dus 11,18%.


